جدول المحتويات
مجهودات العلماء في تطوير النموذج الذري، منذ اكتشاف الذرة، عمل العلماء بجد على تطوير فهمنا للنموذج الذري. تضمن ذلك نموذج بوهر الكلاسيكي ونموذج شرودنجر الكمومي وهناك تطور في هذا النموذج ليشمل الإلكترونات والبروتونات والنيوترونات وتفاعلاتها داخل الذرة، وأدى إلى تطوير الفهم العميق للبنية الذرية وتفاعلاتها، حيث في مقال اليوم سوف نتعرف بشكل مفصل حول النموذج الذري وما هو والمزيد من جهود العلماء في هذا المجال.
ما هو النموذج الذري؟
- نواة الذرة: تتألف من البروتونات والنيوترونات. البروتونات تحمل شحنة موجبة وتحدد هوية العنصر الكيميائي، بينما النيوترونات ليست لديها شحنة كهربائية وتساهم في استقرار النواة.
- الإلكترونات: تدور حول النواة في مدارات مختلفة. تحمل الإلكترونات شحنة سالبة وتشارك في التفاعلات الكيميائية وتحدد خصائص التكوين الكيميائي والسلوك للعناصر.
- المستويات الطاقية: تصف مواقع وطاقات الإلكترونات حول النواة. تنظم هذه المستويات الطاقية تفاعلات الإلكترونات وقدرتها على الانتقال بين المدارات.
- العدد الذري: هو عدد البروتونات في نواة الذرة ويحدد هوية العنصر. على سبيل المثال، الهيدروجين له عدد ذري 1 بينما للكربون عدد ذري 6.
- العدد الكتلي: هو مجموع البروتونات والنيوترونات في نواة الذرة. يستخدم لحساب وزن ذري نوعي أكثر دقة.
- العناصر والجدول الدوري: يتكون كل عنصر كيميائي من ذرات تحمل نفس العدد الذري. ينظم الجدول الدوري العناصر حسب ترتيبها الكيميائي، حيث يتزايد العدد الذري من يسار الجدول إلى اليمين.
- التكوين الإلكتروني: يصف كيفية توزيع الإلكترونات حول المدارات. يساعد هذا التكوين في توضيح خصائص العنصر الكيميائي وتفاعلاته.
مجهودات العلماء في تطوير النموذج الذري
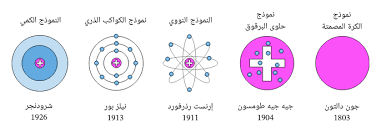
قدم العلماء مجهود هائل على مر العقود لتطوير النموذج الذري وفهم بنية الذرات وفيما يلي بعض المحطات الرئيسية في هذا المجال:
- نموذج بوهر الذري: في عام 1913، قام نيلز بوهر بتطوير نموذج يصف الذرة كنظام شمسي مصغر، حيث تدور الإلكترونات حول النواة في مدارات محددة.
- نموذج شرودنجر: في عام 1926، طور إرفين شرودنجر نموذج يستند إلى المعادلة الموجية، مما أتاح لنا فهم أعمق لتوزيع الإلكترونات حول النواة وظاهرة التراكب الموجي.
- نموذج القاعدة الأربعة: في عام 1927، أقام ويرنر هايزنبيرغ وماكس بورن وباسكال جوردان نموذج القاعدة الأربعة الذي أسهم في فهم التفاعلات الكمومية داخل الذرات.
- مبدأ الاستبدال الإشعاعي: في عام 1930، طور وولفغانغ بولي نموذج يعتمد على مبدأ الاستبدال الإشعاعي، والذي يشرح كيفية امتصاص وإطلاق الإلكترونات للأشعة.
- نموذج القشرة الإلكترونية: في الخمسينات والستينات، تطور فهمنا لبنية الذرات والعناصر بفضل نموذج القشرة الإلكترونية، الذي يصف توزيع الإلكترونات في طبقات مختلفة حول النواة.
اهم العلماء الذين بحثوا في نموذج الذرة
أن هناك العديد من العلماء الذين ساهموا في بحث وتطوير نموذج الذرة على مر العقود و من بعض أهم هؤلاء العلماء:
جون تومسون (1856-1940): اكتشف الإلكترونات واقترح نموذج الذرة “العَشَبِي” أو نموذج الكوكتيل الذي يصف الذرة على أنها جسيم موجب الشحنة مع إلكترونات موزعة داخله.
إرنست رذرفورد (1871-1937): أجرى تجربة الرشفورد بمساعدة طالبه إرنست مارسدن للتأكد من توزيع الشحنة في الذرة اقترح نموذج الذرة النووي حيث تكون معظم الكتلة والشحنة الموجبة في نواة صغيرة في المركز.
نيلز بور (1885-1962): ساهم بشكل كبير في تطوير نموذج الذرة النووي ونموذج الإلكترونات المحددة، وهذا يعني أن الإلكترونات تدور في مدارات محددة حول النواة.
هنري موزلي (1887-1981): قدم نموذج القشرة الإلكترونية الذي أوضح كيف يتم توزيع الإلكترونات في مستويات طاقة مختلفة حول النواة.
النموذج الذري هو تصور علمي يصف بنية الذرة وتكوينها. يشير إلى أن الذرة تتكون من نواة مركزية تحتوي على بروتونات ونيوترونات وتحيط بها مستويات مدارية تحوي الإلكترونات و قد تطور هذا النموذج على مر العقود وساهم في فهمنا للتفاعلات الكيميائية والتكوين الدقيق للعناصر الكيميائية.